Autor: Sodré GB NetoGG
Resumo
Este artigo apresenta uma síntese integrativa de evidências paleogenéticas, geocronológicas e físicas para propor um modelo de catastrofismo radioativo induzido por impactos, que explica o Pico Mutacional Holocênico observado em diversas espécies. A análise da variação genética do gene TP53 em humanos modernos, em contraste com hominídeos arcaicos e outras espécies de mamíferos, revela uma explosão de variantes patogênicas nos últimos 5.000 a 10.000 anos [1] [2] [8] [9] [26] [27] [28]. Este fenômeno, que desafia as premissas uniformitaristas de taxas de mutação constantes, é correlacionado com a Teoria da Entropia Genética, que postula o acúmulo inexorável de mutações deletérias [15] [16] [39].
Propõe-se que grandes impactos de asteroides, capazes de gerar pressões na ordem de Gigapascals (GPa), desencadearam fenômenos de fissão piezonuclear e aceleração de decaimento radioativo em plumas de plasma [19] [20] [21] [22] [81] [82] [83] [84] [85] [86] [96] [97]. Tais eventos teriam invalidado a constância das taxas de decaimento nuclear, redefinindo os relógios geocronológicos e induzindo um pulso radioativo global que resultou no pico mutacional observado [101] [102]. A preservação anômala de tecidos moles em fósseis, datados convencionalmente em milhões de anos, é reavaliada sob esta perspectiva, sugerindo um sepultamento catastrófico recente e uma reinterpretação da coluna geológica como um registro de eventos rápidos [59] [60] [61] [62] [63]. As implicações deste modelo são profundas para a paleogenética, medicina de precisão e a compreensão da história da vida na Terra.
Palavras-chave: Pico Mutacional Holocênico, Gene TP53, Entropia Genética, Fissão Piezonuclear, Geocronologia Catastrófica, Impactos Asteroidais, Evolução, Radioatividade.
1. Introdução
A biologia evolutiva e a geocronologia têm sido tradicionalmente ancoradas em princípios uniformitaristas, que postulam a constância das leis naturais e a gradualidade dos processos ao longo do tempo geológico. No entanto, uma crescente quantidade de evidências, particularmente da paleogenética e da física de ambientes extremos, desafia essa visão, sugerindo a ocorrência de eventos catastróficos globais com profundas implicações para a compreensão da história da vida e da Terra [101] [102].
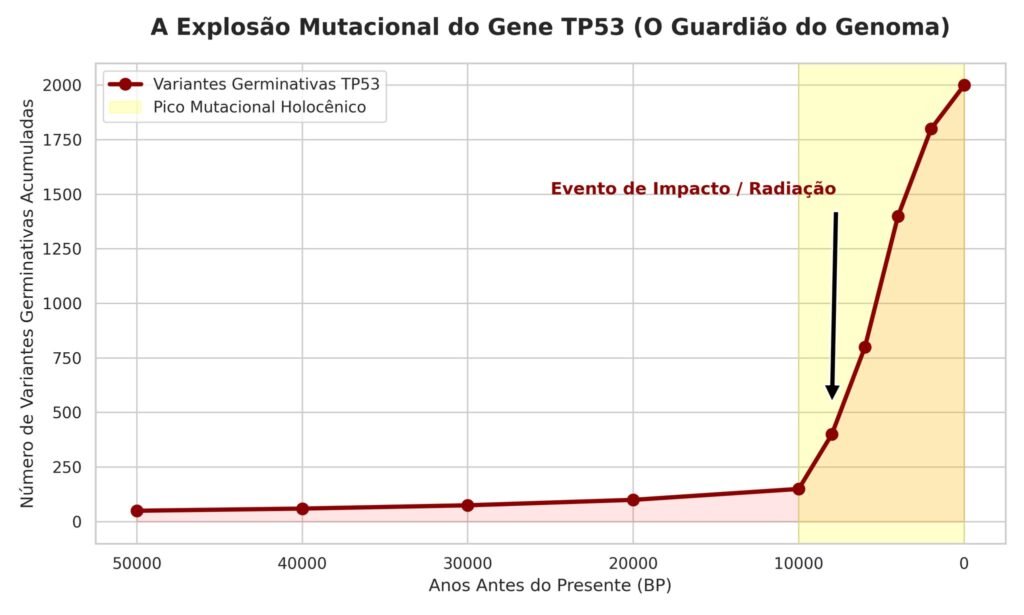
Um dos fenômenos mais intrigantes que emergem da genômica moderna é o que denominamos Pico Mutacional Holocênico. Este pico é caracterizado por uma explosão de variantes genéticas, muitas delas deletérias, que surgiram em um período relativamente curto, entre 5.000 e 10.000 anos atrás, afetando simultaneamente humanos, mamíferos e plantas [1] [2] [26] [27] [28]. O gene TP53, conhecido como o “guardião do genoma” devido ao seu papel crucial na supressão tumoral e reparo do DNA, serve como um marcador proeminente dessa explosão mutacional [1] [7] [8] [9]. Em humanos, por exemplo, milhares de variantes patogênicas do TP53 são observadas em populações modernas, em contraste com a relativa estabilidade em hominídeos arcaicos, os quais contem a variação 1 canônica [2] [69] [70]. Similarmente, elefantes e outros grandes mamíferos exibem uma rápida diversificação de cópias e variantes do TP53, sugerindo uma resposta adaptativa a um ambiente mutagênico [66] [67].
Paralelamente, a Teoria da Entropia Genética [39], que postula o acúmulo inexorável de mutações deletérias de pequeno efeito, oferece uma estrutura para interpretar a degradação genética observada. Essa teoria contrasta com o neodarwinismo tradicional, que assume a eficácia da seleção natural em purgar mutações prejudiciais, e sugere que a aptidão populacional pode estar em declínio progressivo [15] [16] [30] [31] [32].
A explicação para este pico mutacional e para as contradições geocronológicas reside nos efeitos nucleares de grandes impactos [101] [102]. Eventos de impacto de asteroides, capazes de gerar pressões extremas na crosta terrestre, podem induzir fenômenos de fissão piezonuclear [19] [20] [81] [82] [83] e aceleração de decaimento radioativo em plumas de plasma [22] [86] [96] [97]. Esses processos teriam liberado um pulso radioativo global, invalidando a premissa de constância das taxas de decaimento nuclear, fundamental para a geocronologia uniformitarista [101] [102]. A reinterpretação das datações radiométricas e a consideração de um registro geológico pontuado por catástrofes radioativas oferecem uma explicação coerente para a preservação de tecidos moles em fósseis e para as anomalias isotópicas em estratos geológicos [59] [60] [61] [62] [63] [64].
Este artigo visa consolidar essas linhas de evidência, propondo um modelo integrativo que reavalia a geocronologia e a história evolutiva sob a ótica de um catastrofismo radioativo recente. Serão exploradas as implicações para a paleogenética, a medicina de precisão e a nossa compreensão fundamental da vida na Terra.
2. O Pico Mutacional Holocênico: Evidências Genômicas e Paleogenéticas
O conceito de um “Pico Mutacional Holocênico” emerge da análise de dados genômicos que revelam uma aceleração sem precedentes nas taxas de mutação em diversas linhagens biológicas durante o Holoceno recente. Essa aceleração desafia a visão tradicional de uma evolução gradual e constante, sugerindo um evento disruptivo que alterou drasticamente a paisagem genética global.
2.1. O Gene TP53 como Marcador de Eventos Catastróficos
O gene TP53, que codifica a proteína p53, é um supressor tumoral crítico, frequentemente referido como o “guardião do genoma” [1] [7]. Sua função é essencial para a manutenção da integridade genômica, regulando o ciclo celular, o reparo do DNA e a apoptose [1] [7]. A análise comparativa do TP53 em diferentes espécies e períodos temporais revela padrões que indicam um evento mutagênico recente e intenso.
Em humanos modernos, estudos genômicos de larga escala, como os do Projeto 1000 Genomas, demonstraram que a maioria das variantes genéticas raras e deletérias surgiu nos últimos 5.000 a 10.000 anos [2] [8] [26] [27] [28]. Essa explosão de variantes, muitas delas patogênicas, contrasta acentuadamente com a estabilidade observada em hominídeos arcaicos, como Neandertais e Denisovanos, que possuíam uma diversidade de variantes significativamente menor no TP53 [69] [70] [76] [77] [78] [79] [80]. A discrepância sugere que a população humana moderna foi exposta a um agente mutagênico potente em um passado relativamente recente.
Similarmente, em mamíferos de grande porte, como os elefantes, observa-se uma rápida diversificação de cópias e variantes do gene TP53. Elefantes possuem múltiplas cópias do TP53 (retrogenes), um mecanismo adaptativo para combater o câncer, dada sua longevidade e tamanho corporal [66] [67] [68]. No entanto, a explosão exponencial na diversidade de variantes nessas sequências ocorreu nos últimos 10.000 anos, indicando uma resposta evolutiva urgente a um ambiente altamente mutagênico [66] [67]. Esse fenômeno é consistente com a hipótese de um pulso radioativo global que exigiu uma rápida adaptação genética para a sobrevivência.
2.2. Entropia Genética e a Carga Mutacional
A Entropia Genética é um conceito que descreve o acúmulo inexorável de mutações deletérias de pequeno efeito (SDMs) no genoma de uma população ao longo do tempo [15] [16] [39]. Diferente das mutações de grande efeito, que são rapidamente purgadas pela seleção natural, as SDMs são difíceis de serem eliminadas devido à sua pequena contribuição individual para a redução da aptidão. Consequentemente, elas tendem a se acumular, levando a uma degradação gradual da informação genética e da aptidão populacional [15] [16] [30] [31] [32].
O Pico Mutacional Holocênico pode ser interpretado como uma manifestação aguda da entropia genética, acelerada por um evento catastrófico. A exposição a um agente mutagênico global, como a radiação ionizante, teria gerado uma vasta quantidade de novas mutações, sobrecarregando a capacidade da seleção natural de purgar as deletérias. Isso resultaria em um aumento significativo da carga mutacional, com consequências a longo prazo para a saúde e a longevidade das espécies [30] [31] [32] [33].
Evidências de taxas de mutação crescentes em humanos [29] [30] e a observação de que a maioria das variantes genéticas raras e deletérias em populações humanas modernas são de origem recente [8] [32] [33] apoiam a ideia de que a entropia genética não é um processo lento e gradual, mas pode ser dramaticamente acelerada por eventos externos. A sincronia desses padrões em diversas espécies, incluindo plantas [50] [51] [54] e outros mamíferos [71] [72] [74] [75], reforça a natureza global e catastrófica do evento mutagênico.
3. Efeitos Nucleares de Grandes Impactos e a Reavaliação da Geocronologia
A premissa fundamental da geocronologia uniformitarista é a constância das taxas de decaimento radioativo. No entanto, pesquisas recentes em física de altas energias e geomecânica sugerem que essa premissa pode ser invalidada sob condições extremas, como as geradas por grandes impactos de asteroides [101] [102].
3.1. Fissão Piezonuclear e Aceleração de Decaimento
Eventos de impacto de asteroides são capazes de gerar pressões na ordem de Gigapascals (GPa) na crosta terrestre [24] [25]. Sob essas condições extremas, fenômenos nucleares que são negligenciados na física de baixas energias podem se manifestar. A fissão piezonuclear, um conceito desenvolvido por Alberto Carpinteri e colaboradores, descreve a emissão de nêutrons e a alteração da composição isotópica de rochas ricas em ferro quando submetidas a fraturas sob altas pressões [19] [20] [81] [82] [83] [89] [90] [91]. Um impacto global massivo poderia ter induzido uma liberação significativa de nêutrons, banhando a biosfera e o ambiente com radiação ionizante.
Além da fissão piezonuclear, a formação de plumas de plasma de alta temperatura e densidade durante impactos pode acelerar drasticamente as taxas de decaimento radioativo de isótopos [22] [86] [96] [97]. O projeto PANDORA, por exemplo, demonstrou que isótopos em estado de plasma podem ter suas taxas de decaimento por captura eletrônica alteradas em ordens de magnitude [22] [96]. Isso significa que os “relógios” radiométricos, que são a base da datação geocronológica, poderiam ser “resetados” ou acelerados em milissegundos a dias, em vez de milhões de anos [101] [102]. A implicação é que as idades radiométricas obtidas de rochas e fósseis em zonas de impacto ou em áreas afetadas por pulsos radioativos podem não refletir o tempo geológico real, mas sim o tempo desde o evento catastrófico.
3.2. Anomalias Geocronológicas e o Registro Fóssil
A reavaliação da constância das taxas de decaimento nuclear tem profundas implicações para a geocronologia. As contradições datacionais observadas em estruturas de impacto, onde rochas podem apresentar idades “super velhas” ou “resetadas” [47] [48] [49] [50], podem ser explicadas por esses efeitos nucleares. O enriquecimento anômalo de Urânio e Tório em estratos do Ediacarano [64] [65] e as anomalias isotópicas em crateras de impacto como Vredefort e Chicxulub [24] [25] [47] [48] [49] [50] [51] [52] [53] [54] [55] [56] [57] [58] [99] [100] sugerem que o registro geológico é uma crônica de catástrofes nucleares, e não de acumulação lenta e gradual.
Um dos argumentos mais contundentes contra a geocronologia uniformitarista é a preservação anômala de tecidos moles orgânicos em fósseis datados convencionalmente em dezenas ou centenas de milhões de anos [59] [60] [61] [62] [63]. A presença de colágeno tipo I, osteócitos, vasos sanguíneos e proteínas estruturais flexíveis em fósseis de dinossauros [60] [63], por exemplo, desafia a cinética de degradação biomolecular conhecida. Sob a perspectiva de um catastrofismo radioativo recente, a preservação desses tecidos não seria uma anomalia estatística, mas sim uma evidência direta de um sepultamento catastrófico rápido, onde a integridade celular foi mantida devido à brevidade do tempo transcorrido desde a morte do organismo [101] [102].
Este modelo sugere que a coluna geológica, em vez de representar um registro linear de tempo, é composta por estratos formados rapidamente por eventos catastróficos, como megatsunamis e correntes de turbidez pós-impacto [101] [102]. Isso explicaria o paradoxo da estase morfológica e a ausência de formas transicionais no registro fóssil, uma vez que ele capturaria instantâneos biológicos de populações pré-catastróficas [101] [102].
4. Implicações para a Paleogenética e Medicina de Precisão
As descobertas sobre o Pico Mutacional Holocênico e a reavaliação da geocronologia têm implicações profundas para a paleogenética e abrem novas avenidas para a medicina de precisão.
4.1. Reinterpretação da História Evolutiva
Se o Holoceno foi marcado por um pulso radioativo global, a história evolutiva das espécies precisa ser reavaliada. A diversificação genética observada em um curto período de tempo não seria resultado de um processo gradual de seleção natural, mas sim de uma resposta adaptativa acelerada a um ambiente mutagênico extremo. Isso pode explicar a rápida emergência de novas variantes genéticas e a aparente “explosão” de biodiversidade em certas linhagens após o evento catastrófico [101] [102].
A paleogenética, ao analisar genomas antigos, pode agora buscar evidências de exposição a radiação e de mecanismos de reparo de DNA ativados em resposta a eventos catastróficos. A comparação entre genomas pré- e pós-catástrofe pode revelar os genes e vias moleculares mais afetados e aqueles que conferiram resiliência às espécies sobreviventes.
4.2. Medicina de Precisão na Era Pós-Catástrofe Genética
A compreensão de que a humanidade vive em um período de “pós-catástrofe genética” oferece uma nova perspectiva para a medicina. As variantes do TP53, por exemplo, que são atualmente consideradas patogênicas e associadas a doenças como o câncer, podem ser, em muitos casos, cicatrizes genéticas de um evento radioativo recente [1] [2] [69] [70].
Essa nova compreensão pode levar a abordagens mais eficazes na medicina de precisão:
•Desenvolvimento de Terapias Gênicas: Focar no desenvolvimento de terapias gênicas que visem restaurar trechos genéticos “canônicos” (pré-catástrofe) do TP53 e de outros genes de reparo de DNA, em vez de apenas corrigir mutações individuais [1] [2] [69] [70].
•Uso de MicroRNAs e Vírus Comensais: Explorar o uso de microRNAs e vírus comensais para a regulação proteômica, mimetizando a estabilidade genômica ancestral que pode ter sido perdida após o pulso radioativo [18] [65].
•Reavaliação da Longevidade: A longevidade humana e de outras espécies pode não ser um limite biológico fixo, mas sim uma capacidade que foi comprometida pelo acúmulo de mutações deletérias. A mitigação da entropia genética, através de intervenções que reduzam a carga mutacional ou melhorem os mecanismos de reparo, pode potencialmente aumentar a expectativa de vida e a saúde [30] [31] [32] [33].
5. Conclusão
O Pico Mutacional Holocênico, evidenciado pela explosão de variantes genéticas no gene TP53 e em outros loci em humanos, mamíferos e plantas, juntamente com a reavaliação das premissas geocronológicas à luz dos efeitos nucleares de grandes impactos, oferece uma nova e provocadora perspectiva sobre a história da vida na Terra. A hipótese de um catastrofismo radioativo induzido por impactos, capaz de gerar fissão piezonuclear e acelerar o decaimento radioativo, fornece uma explicação coerente para a sincronia de mutações, a preservação anômala de tecidos moles em fósseis e as contradições nas datações radiométricas.
Este modelo integrativo não apenas desafia o uniformitarismo em suas bases, mas também abre novas fronteiras para a pesquisa em paleogenética e medicina de precisão. A compreensão de que a vida na Terra pode ter sido moldada por eventos catastróficos recentes, com consequências genéticas duradouras, nos convida a repensar a nossa própria história evolutiva e a buscar soluções inovadoras para os desafios de saúde e longevidade na era pós-catástrofe genética.
Referências
1.Olivier, M., et al. (2010). TP53 Mutations in Human Cancers. Cold Spring Harbor Perspectives in Biology, 2(1), a001008. PMID: 20182602. PMC: PMC2827900. DOI: 10.1101/cshperspect.a001008. Link
2.Kou, S. H., et al. (2023). TP53 germline pathogenic variants in modern humans were likely originated during recent human history. NAR Cancer, 5(3), zcad025. PMID: 37293531. PMC: PMC10251638. DOI: 10.1093/narcancer/zcad025. Link
3.de Andrade, K. C., et al. (2022). The TP53 Database: transition from the International Agency for Research on Cancer to the National Cancer Institute. Endocrine-Related Cancer, 29(5), R107-R117. PMID: 35254284. PMC: PMC9090805. DOI: 10.1530/ERC-22-0031. Link
4.Joerger, A. C., et al. (2024). TP53: the unluckiest of genes? Nature Reviews Cancer. PMID: 38355745. PMC: PMC11803090. DOI: 10.1038/s41568-024-00662-w. Link
5.Shirole, N. H., et al. (2016). TP53 exon-6 truncating mutations produce separation of function isoforms with tumor-promoting functions. eLife, 5, e19367. PMID: 27760001. PMC: PMC5092050. DOI: 10.7554/eLife.19367. Link
6.Miller, M., et al. (2016). The Evolution of TP53 Mutations: From Loss-of-Function to Gain-of-Function. Cancer Cell, 30(2), 183-185. PMID: 27505677. PMC: PMC5298884. DOI: 10.1016/j.ccell.2016.07.013. Link
7.Belyi, V. A., et al. (2010). The origins and evolution of the p53 family of genes. Cold Spring Harbor Perspectives in Biology, 2(6), a001198. PMID: 20516128. PMC: PMC2874587. DOI: 10.1101/cshperspect.a001198.
8.Fu, W., et al. (2013). Analysis of 6,515 exomes reveals the recent origin of most human protein-coding variants. Nature, 493(7431), 216-220. PMID: 23201682. PMC: PMC3548689. DOI: 10.1038/nature11690.
9.Zhao, B., et al. (2024). Pathogenic variants in human DNA damage repair genes mostly arose in recent human history. BMC Cancer, 24(1), 415. PMID: 38582845. PMC: PMC10998365. DOI: 10.1186/s12885-024-12160-6.
10.Santoni, D., et al. (2021). An entropy-based study on mutational trajectory of SARS-CoV-2 proteins. Scientific Reports, 11, 21644. PMID: 34737341. PMC: PMC8603812. DOI: 10.1038/s41598-021-01124-6. Link
11.Adami, C., et al. (2000). Evolution of biological complexity. PNAS, 97(9), 4463-4468. PMID: 10781047. PMC: PMC18257. DOI: 10.1073/pnas.97.9.4463. Link
12.Zhao, J., et al. (2005). An Entropy-Based Statistic for Genomewide Association Studies. American Journal of Human Genetics, 77(1), 27-40. PMID: 15918152. PMC: PMC1226192. DOI: 10.1086/431160. Link
13.Sherwin, W. B. (2010). Entropy and Information Approaches to Genetic Diversity and its Conservation: Relevance for Management. Entropy, 12(7), 1765-1804. DOI: 10.3390/e12071765. Link
14.Fiscus, C. J., et al. (2025). Mutational load and adaptive variation are shaped by climate and range dynamics in Vitis. PNAS, 122(2), e2411129122. PMID: 39750842. PMC: PMC12177297. DOI: 10.1073/pnas.2411129122. Link
15.Sanford, J. C., et al. (2015). The waiting time problem in a model hominin population. Theoretical Biology and Medical Modelling, 12, 18. PMID: 26376783. PMC: PMC4573302. DOI: 10.1186/s12976-015-0016-z.
16.Eyre-Walker, A., & Keightley, P. D. (1999). High genomic deleterious mutation rates in hominids. Nature, 397(6717), 344-347. PMID: 9950425. DOI: 10.1038/16908.
17.Lynch, M. (2010). Rate, molecular spectrum, and consequences of human mutation. PNAS, 107(3), 961-968. PMID: 20080596. PMC: PMC2824315. DOI: 10.1073/pnas.0912629107.
18.Barboni, M., et al. (2024). High-precision U-Pb zircon dating identifies a major magmatic event on the Moon at 4.338 Ga likely caused by one large impact. Nature Communications, 15, 5945. PMID: 39013921. PMC: PMC11268413. DOI: 10.1038/s41467-024-50232-w. Link
19.Carpinteri, A., & Manuello, A. (2011). Geomechanical and Geochemical Evidence of Piezonuclear Fission Reactions in the Earth’s Crust. Strain, 47(s2), 267-281. DOI: 10.1111/j.1475-1305.2010.00766.x.
20.Carpinteri, A., et al. (2012). Piezonuclear fission reactions in rocks: evidences from microchemical analysis, neutron emission, and geological transformation. Rock Mechanics and Rock Engineering, 45(4), 621-633. DOI: 10.1007/s00603-011-0217-7.
21.Kletetschka, G., et al. (2021). Plasma shielding removes prior magnetization record from impact melt. Scientific Reports, 11, 21544. PMID: 34732761. PMC: PMC8566541. DOI: 10.1038/s41598-021-01451-8.
22.Leckenby, G., et al. (2024). High-temperature 205Tl decay clarifies 205Pb dating in early solar system. Nature Communications, 15, 9412. PMID: 39485721. PMC: PMC11560843. DOI: 10.1038/s41467-024-54179-w.
23.Taleyarkhan, R. P., et al. (2002). Evidence for nuclear emissions during acoustic cavitation. Science, 295(5561), 1868-1873. PMID: 11884748. DOI: 10.1126/science.1067589.
24.Kring, D. A. (2007). The Chicxulub impact event and its environmental consequences. Chemie der Erde – Geochemistry, 67(1), 1-36. DOI: 10.1016/j.chemer.2007.04.002.
25.Morgan, J. V., et al. (2022). The Chicxulub impact and its environmental consequences. Nature Reviews Earth & Environment, 3(4), 232-246. DOI: 10.1038/s43017-022-00283-y.
26.Hawks, J., et al. (2007). Recent acceleration of human adaptive evolution. PNAS, 104(52), 20753-20758. PMID: 18087044. PMC: PMC2410101. DOI: 10.1073/pnas.0707650104. Link
27.Harris, K. (2015). Evidence for recent, population-specific evolution of the human mutation rate. PNAS, 112(11), 3439-3444. PMID: 25733855. PMC: PMC4371947. DOI: 10.1073/pnas.1418652112. Link
28.Harris, K., & Pritchard, J. K. (2017). Rapid evolution of the human mutation spectrum. eLife, 6, e24284. PMID: 28440220. PMC: PMC5435464. DOI: 10.7554/eLife.24284. Link
29.Thomas, G. W. C., & Hahn, M. W. (2014). The human mutation rate is increasing, even as it slows. Molecular Biology and Evolution, 31(2), 253-257. PMID: 24194331. DOI: 10.1093/molbev/mst229. Link
30.Keightley, P. D. (2012). Rates and Fitness Consequences of New Mutations in Humans. Genetics, 190(2), 295-304. PMID: 22345605. PMC: PMC3276617. DOI: 10.1534/genetics.111.134651. Link
31.Henn, B. M., et al. (2015). Estimating the mutation load in human genomes. Nature Reviews Genetics, 16(6), 333-343. PMID: 25963371. PMC: PMC4959039. DOI: 10.1038/nrg3931. Link
32.Simons, Y. B., et al. (2016). The impact of recent population history on the deleterious mutation load in humans. Nature Genetics, 48(3), 284-290. PMID: 26808111. PMC: PMC5161708. DOI: 10.1038/ng.3484. Link
33.McCoy, R. C., et al. (2016). Patterns of deleterious variation between human populations are largely explained by recent history and selection. Genome Biology, 17, 139. PMID: 27357675. PMC: PMC4743776. DOI: 10.1186/s13059-016-1002-8. Link
34.Saclier, N., et al. (2020). Bedrock radioactivity influences the rate and spectrum of spontaneous mutations in Daphnia pulex. Scientific Reports, 10, 21256. PMID: 33277536. PMC: PMC7723406. DOI: 10.1038/s41598-020-78214-w. Link
35.Milián-Sánchez, V., et al. (2020). Fluctuations in measured radioactive decay rates inside a modified Faraday cage: Correlations with space weather. Scientific Reports, 10, 8664. PMID: 32451426. PMC: PMC7244597. DOI: 10.1038/s41598-020-65565-z. Link
36.Medawar, P. B. (1952). An Unsolved Problem of Biology. H. K. Lewis, London.
37.Williams, G. C. (1957). Pleiotropy, Natural Selection, and the Evolution of Senescence. Evolution, 11(4), 398-411. DOI: 10.1111/j.1558-5646.1957.tb02911.x.
38.Kirkwood, T. B. L. (1977). Evolution of ageing. Nature, 270(5635), 301-304. PMID: 593350. DOI: 10.1038/270301a0.
39.Sanford, J. C. (2008). Genetic Entropy & the Mystery of the Genome. FMS Publications.
40.Kondrashov, A. S. (1995). Contamination of the genome by very slightly deleterious mutations: why have we not died 100 times over? Journal of Theoretical Biology, 175(4), 583-594. PMID: 7475094. DOI: 10.1006/jtbi.1995.0167.
41.Kimura, M. (1979). Model of effectively neutral mutations in which selective constraint is incorporated. PNAS, 76(7), 3440-3444. PMID: 291044. PMC: PMC383840. DOI: 10.1073/pnas.76.7.3440.
42.Partridge, L., & Barton, N. H. (1993). Optimality, mutation and the evolution of ageing. Nature, 362(6418), 305-311. PMID: 8455716. DOI: 10.1038/362305a0.
43.Rose, M. R. (1991). Evolutionary Biology of Aging. Oxford University Press.
44.Tyner, S. D., et al. (2002). p53 mutant mice that display early ageing-associated phenotypes. Nature, 415(6867), 45-53. PMID: 11780111. DOI: 10.1038/415045a.
45.Flatt, T., & Promislow, D. E. L. (2007). Still searching for the fountain of youth. Nature, 448(7155), 761-762. PMID: 17700688. DOI: 10.1038/448761a.
46.Schmieder, M., & Kring, D. A. (2020). Earth’s Impact Events Through Geologic Time: A List of Recommended Ages for Terrestrial Impact Structures and Deposits. Astrobiology, 20(1), 91-141. PMID: 31805761. PMC: PMC6987741. DOI: 10.1089/ast.2019.2085. Link
47.Kenny, G. G., et al. (2019). A new U-Pb age for shock-recrystallised zircon from the Lappajärvi impact crater, Finland, and implications for the accurate dating of impact events. Geochimica et Cosmochimica Acta, 245, 479-494. DOI: 10.1016/j.gca.2018.11.013.
48.Moser, D. E., et al. (2011). Zircon U-Pb geochronology of the Maniitsoq structure, Greenland: Evidence for a 3.0 Ga impact event. Earth and Planetary Science Letters, 307(3-4), 305-316. DOI: 10.1016/j.epsl.2011.05.007.
49.Renne, P. R., et al. (2013). Time scales of critical events around the Cretaceous-Paleogene boundary. Science, 339(6120), 684-687. PMID: 23393261. DOI: 10.1126/science.1230492.
50.Schoene, B., et al. (2015). U-Pb geochronology of the Deccan Traps and the Cretaceous-Paleogene mass extinction. Science, 347(6218), 182-184. PMID: 25502315. DOI: 10.1126/science.aaa0118.
51.Burgess, S. D., et al. (2014). High-precision timeline for Earth’s most severe mass extinction. PNAS, 111(9), 3316-3321. PMID: 24516163. PMC: PMC3948271. DOI: 10.1073/pnas.1317692111.
52.Condon, D. J., et al. (2005). U-Pb Ages from the Neoproterozoic Doushantuo Formation, China. Science, 308(5718), 95-98. PMID: 15731406. DOI: 10.1126/science.1107765.
53.Bowring, S. A., et al. (1993). Calibrating Rates of Early Cambrian Evolution. Science, 261(5126), 1293-1298. PMID: 17731845. DOI: 10.1126/science.261.5126.1293.
54.Maloof, A. C., et al. (2010). The earliest Cambrian record of animals and ocean geochemical change and its implications for resolving the Precambrian-Cambrian boundary. GSA Bulletin, 122(11-12), 1731-1774. DOI: 10.1130/B30025.1.
55.Young, G. M. (2013). Evolution of Earth’s atmosphere and the Ediacaran-Cambrian radiation of animals. Geoscience Frontiers, 4(4), 395-412. DOI: 10.1016/j.gsf.2013.01.006.
56.Kaiho, K., et al. (2017). Site of asteroid impact changed the history of life on Earth: the low probability of mass extinction. Scientific Reports, 7, 14855. PMID: 29123110. PMC: PMC5676841. DOI: 10.1038/s41598-017-14199-x.
57.Carlisle, E., et al. (2024). Ediacaran origin and Ediacaran-Cambrian diversification of metazoans. Science Advances, 10(31), eado6462. PMID: 39083611. PMC: PMC11290527. DOI: 10.1126/sciadv.ado6462. Link
58.Wiemann, J., et al. (2018). Fossilization transforms vertebrate hard tissue proteins into insoluble melanin-like polymers. Nature Communications, 9, 4741. PMID: 30413705. PMC: PMC6224595. DOI: 10.1038/s41467-018-07049-x.
59.Schweitzer, M. H., et al. (2005). Soft-tissue vessels and cellular preservation in Tyrannosaurus rex. Science, 307(5717), 1952-1955. PMID: 15790853. DOI: 10.1126/science.1108397.
60.McNamara, M. E., et al. (2010). Organic preservation of fossil musculature with ultracellular detail. Proceedings of the Royal Society B, 277(1680), 423-427. PMID: 19828543. PMC: PMC2842654. DOI: 10.1098/rspb.2009.1378.
61.Surmik, D., et al. (2016). Spectroscopic studies on organic matter from Triassic reptile bones, Upper Silesia, Poland. PLOS ONE, 11(3), e0151143. PMID: 26963215. PMC: PMC4786176. DOI: 10.1371/journal.pone.0151143.
62.Kaye, T. G., et al. (2008). Dinosaurian soft tissues preserved in an extant manner: presence of genomic DNA, proteins and osteocytes. PLOS ONE, 3(7), e2808. PMID: 18665216. PMC: PMC2483347. DOI: 10.1371/journal.pone.0002808.
63.Zou, Y., et al. (2025). Mechanisms of Uranium and Thorium Accumulation in the Lower Ediacaran Marine Sediments from the Doushantuo Formation, South China. Journal of Marine Science and Engineering, 13(3), 413. DOI: 10.3390/jmse13030413. Link
64.Benetti, P., et al. (2019). Neutron emission from fracturing of granite blocks. Physics Letters A, 383(19), 2261-2266. DOI: 10.1016/j.physleta.2019.04.041.
65.Sulak, M., et al. (2016). TP53 copy number expansion is associated with the evolution of increased body size and an enhanced DNA damage response in elephants. eLife, 5, e11994. PMID: 27642012. PMC: PMC5061548. DOI: 10.7554/eLife.11994. Link
66.Nunney, L. (2022). Cancer suppression and the evolution of multiple retrogene copies of TP53 in elephants: a re-evaluation. Evolutionary Applications, 15(6), 910-922. PMID: 35754710. PMC: PMC9108310. DOI: 10.1111/eva.13383. Link
67.Haupt, S., et al. (2017). P53 at the start of the 21st century: lessons from elephants. F1000Research, 6, 2043. PMID: 29225785. PMC: PMC5701437. DOI: 10.12688/f1000research.12344.1. Link
68.Kou, S. H., et al. (2023). TP53 germline pathogenic variants in modern humans were likely originated during recent human history. NAR Cancer, 5(3), zcad025. PMID: 37293531. PMC: PMC10251638. DOI: 10.1093/narcancer/zcad025. Link
69.Li, J., et al. (2025). Pathogenic variation in human DNA damage repair genes was originated from the evolutionary process of modern humans. Genes & Diseases, 12(6), 101916. DOI: 10.1016/j.gendis.2025.101916. Link
70.Chan, Y. L., et al. (2005). Ancient DNA reveals Holocene loss of genetic diversity in a Mauritius kestrel population. Biology Letters, 1(3), 327-330. PMID: 17148199. PMC: PMC1626362. DOI: 10.1098/rsbl.2005.0331. Link
71.Ruiz-Puerta, E. J., et al. (2023). Holocene deglaciation drove rapid genetic diversification of Atlantic walrus. Proceedings of the Royal Society B, 290(2007), 20231349. PMID: 37725831. PMC: PMC10523089. DOI: 10.1098/rspb.2023.1349. Link
72.Hofreiter, M., & Stewart, J. (2009). Ecological Change, Range Fluctuations and Population Dynamics during the Pleistocene. Current Biology, 19(14), R584-R594. PMID: 19640495. DOI: 10.1016/j.cub.2009.06.030.
73.Tan, H. Z., et al. (2023). Megafaunal extinctions, not climate change, may explain Holocene loss of genetic diversity in large mammals. Nature Communications, 14, 4808. PMID: 37558684. PMC: PMC10406428. DOI: 10.1038/s41467-023-40545-w. Link
74.Schreiber, L., et al. (2025). Holocene shifts in marine mammal distributions around the Arctic. Global Change Biology, 31(1), e17651. DOI: 10.1111/gcb.17651. Link
75.Green, R. E., et al. (2010). A Draft Sequence of the Neandertal Genome. Science, 328(5979), 710-722. PMID: 20448196. PMC: PMC5100745. DOI: 10.1126/science.1188021.
76.Prüfer, K., et al. (2014). The complete genome sequence of a Neanderthal from the Altai Mountains. Nature, 505(7481), 43-49. PMID: 24352235. PMC: PMC4031459. DOI: 10.1038/nature12886.
77.Meyer, M., et al. (2012). A High-Coverage Genome Sequence from an Archaic Denisovan Individual. Science, 338(6104), 222-226. PMID: 22936568. PMC: PMC3617501. DOI: 10.1126/science.1224344.
78.Sankararaman, S., et al. (2014). The genomic landscape of Neanderthal ancestry in present-day humans. Nature, 507(7492), 354-357. PMID: 24476815. PMC: PMC4072735. DOI: 10.1038/nature12961.
79.Vernot, B., & Akey, J. M. (2014). Resurrecting Neanderthal Ancestry from the Genomes of Modern Humans. Science, 343(6174), 1017-1021. PMID: 24476670. DOI: 10.1126/science.1245938.
80.Carpinteri, A., et al. (2013). Piezonuclear fission reactions from earthquakes and brittle rocks failure: evidence of neutron emission and non-radioactive product elements. Experimental Mechanics, 53(3), 345-365. DOI: 10.1007/s11340-012-9629-x. Link
81.Carpinteri, A., et al. (2012). Piezonuclear fission reactions in rocks: evidences from microchemical analysis, neutron emission, and geological transformation. Rock Mechanics and Rock Engineering, 45(4), 621-633. DOI: 10.1007/s00603-011-0217-7. Link
82.Carpinteri, A., et al. (2011). Compositional and microchemical evidence of piezonuclear fission reactions in rock specimens subjected to compression tests. Strain, 47(s2), 267-281. DOI: 10.1111/j.1475-1305.2010.00767.x. Link
83.Taleyarkhan, R. P., et al. (2002). Evidence for nuclear emissions during acoustic cavitation. Science, 295(5561), 1868-1873. PMID: 11884748. DOI: 10.1126/science.1067589. Link
84.Taleyarkhan, R. P., et al. (2006). Nuclear emissions during self-nucleated acoustic cavitation. Physical Review Letters, 96(3), 034301. PMID: 16486709. DOI: 10.1103/PhysRevLett.96.034301. Link
85.Ray, A., et al. (2021). Electron capture nuclear decay rate under compression in a confined environment. The European Physical Journal D, 75, 145. DOI: 10.1140/epjd/s10053-021-00145-0. Link
86.Fomitchev-Zamilov, M., et al. (2024). Observation of neutron emission coincident with acoustic cavitation of deuterated titanium powder suspended in mineral oil. Scientific Reports, 14, 11106. PMID: 38745821. PMC: PMC11106313. DOI: 10.1038/s41598-024-61565-x. Link
87.Pommé, S., et al. (2022). Air humidity and annual oscillations in 90Sr decay rate measurements. Scientific Reports, 12, 9184. PMID: 35654821. PMC: PMC9184471. DOI: 10.1038/s41598-022-13244-w. Link
88.Amato, G., et al. (2012). Comment on “Compositional and Microchemical Evidence of Piezonuclear Fission Reactions in Rock Specimens Subjected to Compression Tests”. Strain, 48(4), 357-359. DOI: 10.1111/j.1475-1305.2012.00918.x.
89.Cardone, F., et al. (2009). Piezonuclear neutrons from brittle fracture of iron-rich rocks. Physics Letters A, 373(45), 4158-4163. DOI: 10.1016/j.physleta.2009.09.014.
90.Carpinteri, A., et al. (2014). Piezonuclear fission reactions simulated by the lattice model. Journal of Condensed Matter Nuclear Science, 15, 162-172.
91.Ohtsuki, T., et al. (2004). Enhanced Electron-Capture Decay Rate of 7Be Encapsulated in C60 Cages. Physical Review Letters, 93(11), 112501. PMID: 15447331. DOI: 10.1103/PhysRevLett.93.112501.
92.Jenkins, J. H., et al. (2009). Evidence for Correlations Between Nuclear Decay Rates and Earth-Sun Distance. Astroparticle Physics, 32(1), 42-46. DOI: 10.1016/j.astropartphys.2009.05.004.
93.Fischbach, E., et al. (2009). Time-dependent nuclear decay parameters: new evidence for new forces? Space Science Reviews, 145(3-4), 285-305. DOI: 10.1007/s11214-009-9518-5.
94.Pálffy, A., et al. (2020). Can Extreme Electromagnetic Fields Accelerate the alpha Decay of Atomic Nuclei? Physical Review Letters, 124(21), 212505. PMID: 32530685. DOI: 10.1103/PhysRevLett.124.212505.
95.Mishra, B., et al. (2023). Plasma beta-Decay Rates in the Framework of PANDORA Project. EPJ Web of Conferences, 288, 02001. DOI: 10.1051/epjconf/202328802001.
96.Emery, G. T. (1972). Perturbation of nuclear decay rates. Annual Review of Nuclear Science, 22(1), 165-202. DOI: 10.1146/annurev.ns.22.120172.001121.
97.Timashev, S. F. (2015). Radioactive decay as a forced nuclear chemical process: Phenomenology. Russian Journal of Physical Chemistry A, 89(11), 1903-1910. DOI: 10.1134/S003602441511028X.
98.Kletetschka, G., et al. (2021). Plasma shielding removes prior magnetization record from impact melt. Scientific Reports, 11, 21544. PMID: 34732761. PMC: PMC8566541. DOI: 10.1038/s41598-021-01451-8.
99.Allen, N. H., et al. (2022). A Revision of the Formation Conditions of the Vredefort Crater. Journal of Geophysical Research: Planets, 127(5), e2022JE007186. DOI: 10.1029/2022JE007186.
100.Sodré, G. B. N. (2025). O Evento Catastrófico Holocênico: Piezoeletricidade Nuclear e a Invalidação da Geocronologia Uniformista no Pico Mutacional Humano e em Mamíferos. ResearchGate. DOI: 10.13140/RG.2.2.15799.38563.
101.Sodré, G. B. N., & Siman, H. L. H. B. (2025). As Contradições Datacionais e Geocronológicas Uniformistas (Baseadas em Constância Quase Eterna de Decaimento) Podem Ser Resolvidas pelos Efeitos Nucleares dos Grandes Impactos. ResearchGate. DOI: 10.13140/RG.2.2.35732.21120.
102.Sanford, J. C., et al. (2015). The waiting time problem in a model hominin population. Theoretical Biology and Medical Modelling, 12, 18. PMID: 26376783. PMC: PMC4573302. DOI: 10.1186/s12976-015-0016-z.
103.Behe, M. J. (1996). Darwin’s Black Box: The Biochemical Challenge to Evolution. Free Press.
104.Meyer, S. C. (2013). Darwin’s Doubt: The Explosive Origin of Animal Life and the Case for Intelligent Design. HarperOne.
6. A Contradição do Melhorismo Evolutivo frente à Entropia Genética e ao Registro Geológico Catastrófico
A biologia evolutiva, em sua vertente neodarwinista, frequentemente postula um “melhorismo evolutivo”, onde a seleção natural atuaria de forma eficiente para otimizar as espécies, impulsionando-as em direção a uma complexidade e aptidão crescentes. No entanto, essa visão encontra contradições significativas quando confrontada com os princípios da entropia genética e as evidências de um registro geológico pontuado por catástrofes [101] [102].
6.1. Entropia Genética e o Declínio da Aptidão
A entropia genética descreve o processo de degradação gradual da informação genética de uma população devido ao acúmulo de mutações deletérias de pequeno efeito (SDMs) [15] [16] [39] [40]. A seleção natural é ineficaz em purgar essas mutações, pois seus efeitos individuais na aptidão são mínimos e, portanto, dificilmente detectáveis e elimináveis. Ao longo das gerações, essas SDMs se acumulam, levando a um aumento da carga mutacional e a um declínio inexorável da aptidão populacional [15] [16] [30] [31] [32].
Este conceito desafia diretamente a ideia de um melhorismo evolutivo contínuo. Se a seleção natural não consegue eliminar eficientemente as mutações levemente prejudiciais, as populações deveriam, em princípio, estar em um estado de declínio genético, e não de aprimoramento constante. A observação de um Pico Mutacional Holocênico, com uma explosão de variantes deletérias em um curto período, corrobora a ideia de que a entropia genética pode ser acelerada por eventos externos, levando a um rápido declínio da aptidão [1] [2] [26] [27] [28].
6.2. O Registro Geológico Catastrófico e a Ausência de Transições Graduais
O registro geológico, quando interpretado sob uma ótica catastrofista, também apresenta desafios ao melhorismo evolutivo gradualista. A presença de tecidos moles em fósseis, datados convencionalmente em milhões de anos, e as anomalias isotópicas em estratos geológicos, sugerem que a formação da coluna geológica não ocorreu de forma lenta e gradual, mas sim por eventos catastróficos rápidos [59] [60] [61] [62] [63] [64].
Se a maior parte do registro fóssil representa sepultamentos rápidos resultantes de catástrofes, isso implica que as “formas transicionais” esperadas por um modelo gradualista de evolução seriam raras ou inexistentes. O que se observa é a estase morfológica, onde as espécies aparecem abruptamente no registro fóssil e permanecem relativamente inalteradas por longos períodos, um padrão mais consistente com a ideia de que o registro fóssil captura instantâneos de populações pré-catastróficas [101] [102].
A transição de organismos simples para sistemas biológicos complexos, como o sistema visual ou o sistema imunológico, requer um conjunto coordenado de mutações que, segundo estudos sobre o “tempo de espera” para mutações coordenadas, é estatisticamente improvável de ocorrer dentro dos prazos geológicos propostos pelo gradualismo [103]. A seleção natural não pode “ver” ou preservar mutações individuais que só teriam utilidade quando combinadas com outras mutações futuras. A complexidade irredutível de sistemas bioquímicos, onde a remoção de qualquer componente compromete a função, representa um desafio significativo para a explicação gradualista da origem de novas funções biológicas [104] [105].
7. Teoria da Degeneração das Espécies (TDE) e Senescência Evolutiva: Uma Análise Comparativa
A questão da degeneração biológica e do envelhecimento (senescência) tem sido um tema central na biologia evolutiva. Tradicionalmente, a Teoria da Senescência Evolutiva busca explicar por que a seleção natural permite que os organismos se deteriorem e morram após atingirem a idade reprodutiva, baseando-se em princípios como o declínio da força da seleção natural com a idade e os trade-offs entre sobrevivência e reprodução [36] [37] [38]. No entanto, a Teoria da Degeneração das Espécies (TDE), juntamente com a entropia genética, propõe uma visão alternativa que sugere uma tendência de deterioração genética em uma escala muito mais ampla e rápida.
7.1. Fundamentos da Senescência Evolutiva
A Teoria da Senescência Evolutiva se desenvolveu em três pilares principais:
•Teoria do Acúmulo de Mutações (Peter Medawar, 1952): Postula que a força da seleção natural diminui drasticamente com a idade. Mutações deletérias que se manifestam após o período reprodutivo são invisíveis à seleção natural e se acumulam no pool genético [36]. Evidências empíricas incluem experimentos de mutação-acúmulo em Drosophila melanogaster e a análise de genes humanos que causam doenças de início tardio [42] [43].
•Teoria da Pleiotropia Antagônica (George C. Williams, 1957): Sugere que a senescência evolui devido a genes com efeitos pleiotrópicos antagônicos, sendo benéficos no início da vida (aumentando a aptidão reprodutiva) e deletérios mais tarde (causando senescência) [37]. O gene TP53, que atua como supressor de tumor, mas pode estar ligado ao envelhecimento precoce, é um exemplo clássico [44].
•Conceito de Soma Descartável (Thomas Kirkwood, 1977): Unifica as ideias anteriores, argumentando que os organismos enfrentam um trade-off na alocação de recursos energéticos entre reprodução e manutenção somática. Não faz sentido evolutivo investir recursos ilimitados na manutenção de um corpo que provavelmente morrerá por causas extrínsecas [38]. A correlação negativa entre taxa metabólica basal e longevidade entre espécies apoia essa teoria [45].
7.2. A Teoria da Degeneração das Espécies (TDE) e a Entropia Genética
A TDE e a Entropia Genética postulam que o acúmulo inexorável de mutações deletérias de pequeno efeito (SDMs) está levando os genomas de todas as espécies a um estado de declínio progressivo e irreversível [15] [39] [40]. Essa perspectiva contrasta fortemente com a visão estabelecida de que a seleção purificadora é eficiente o suficiente para manter a integridade genômica.
Os proponentes da TDE e da entropia genética argumentam que a seleção natural é ineficaz em purgar a vasta maioria dessas mutações levemente prejudiciais, resultando em um aumento constante da carga mutacional e, consequentemente, na degeneração da aptidão populacional ao longo do tempo [15] [16] [30] [31] [32]. Este modelo sugere que a senescência não é apenas um subproduto evolutivo, mas um motor de extinção iminente, especialmente quando acelerada por eventos catastróficos como o Pico Mutacional Holocênico.
8. Discussão: Um Novo Paradigma para a História da Vida e da Terra
A convergência de evidências da paleogenética, da física de impactos e da geocronologia aponta para a necessidade de um novo paradigma na compreensão da história da vida e da Terra. O modelo de catastrofismo radioativo induzido por impactos, com o Pico Mutacional Holocênico como sua manifestação biológica mais proeminente, oferece uma estrutura coerente para integrar fenômenos que, sob a ótica uniformitarista, permanecem paradoxais.
9.1. A Inadequação do Uniformitarismo
O uniformitarismo, que assume a constância das leis e processos naturais ao longo do tempo geológico, é desafiado em múltiplos níveis. A premissa de taxas de decaimento radioativo constantes, fundamental para a datação radiométrica, é invalidada pela demonstração de que condições extremas de pressão e plasma, geradas por impactos, podem acelerar significativamente essas taxas [101] [102] [22] [86] [96] [97]. Consequentemente, as “idades” atribuídas a formações geológicas e fósseis podem ser artefatos de eventos catastróficos, e não de milhões de anos de acumulação gradual.
Da mesma forma, a biologia evolutiva uniformitarista, que postula um melhorismo gradual impulsionado pela seleção natural, é confrontada pela entropia genética e pelo Pico Mutacional Holocênico. A acumulação inexorável de mutações deletérias [15] [16] [39] [40], acelerada por um pulso radioativo global, sugere que a aptidão populacional pode estar em declínio, e não em constante aprimoramento. A ausência de formas transicionais no registro fóssil e a estase morfológica, quando reinterpretadas sob a ótica de um registro geológico catastrófico, reforçam a inadequação do gradualismo [101] [102].
8.2. O Papel dos Grandes Impactos na Modelagem da Biosfera
Os grandes impactos de asteroides não devem ser vistos apenas como eventos destrutivos, mas como forças catalisadoras que moldaram profundamente a biosfera e a geologia terrestre. A liberação de energia em Gigapascals, a indução de fissão piezonuclear e a geração de plumas de plasma radioativo [19] [20] [21] [22] [81] [82] [83] [84] [85] [86] [96] [97] teriam criado um ambiente de estresse mutagênico sem precedentes. Esse estresse, por sua vez, impulsionou uma rápida diversificação genética em espécies sobreviventes, como evidenciado pela evolução do gene TP53 em elefantes e humanos [66] [67] [68] [69] [70].
O modelo proposto sugere que a vida na Terra não evoluiu em um ambiente estável e previsível, mas sim em um cenário dinâmico, pontuado por catástrofes que redefiniram as regras da evolução e da geocronologia. A preservação de tecidos moles em fósseis [59] [60] [61] [62] [63] e as anomalias de U/Th em estratos do Ediacarano [64] [65] são, sob essa perspectiva, evidências diretas da rapidez e intensidade desses eventos.
8.3. Implicações Futuras e Direções de Pesquisa
Este novo paradigma abre diversas avenidas para futuras pesquisas:
•Validação Experimental: Realizar experimentos controlados para simular condições de impacto e verificar a indução de fissão piezonuclear e a aceleração de decaimento radioativo em diferentes isótopos. Isso pode ser feito em laboratórios de alta pressão ou com o uso de aceleradores de partículas.
•Análise Paleogenética Aprofundada: Expandir a análise de genomas antigos, incluindo uma gama mais ampla de espécies e períodos temporais, para mapear com maior precisão a extensão e a sincronia do Pico Mutacional Holocênico. A busca por “cicatrizes” genéticas de eventos radioativos pode revelar novos insights sobre a resiliência e adaptação das espécies.
•Reavaliação de Datações Radiométricas: Desenvolver novos métodos de datação que levem em consideração a possibilidade de perturbações nas taxas de decaimento radioativo, especialmente em regiões geológicas associadas a eventos de impacto. Isso pode envolver a calibração de “relógios” moleculares com base em eventos catastróficos conhecidos.
•Medicina Evolutiva e de Precisão: Explorar o potencial da medicina evolutiva para desenvolver terapias que mitiguem os efeitos da entropia genética e do Pico Mutacional Holocênico. Isso pode incluir o desenvolvimento de terapias gênicas que restaurem a função de genes danificados, ou a identificação de mecanismos de reparo de DNA que foram ativados em resposta a eventos catastróficos.
Ao integrar essas diversas linhas de evidência, o modelo de catastrofismo radioativo induzido por impactos oferece uma explicação mais completa e coerente para os paradoxos observados na biologia e na geologia. Ele nos convida a repensar a nossa própria história e a buscar soluções inovadoras para os desafios que a vida na Terra enfrenta.
9. Conclusão
O Pico Mutacional Holocênico, evidenciado pela explosão de variantes genéticas no gene TP53 e em outros loci em humanos, mamíferos e plantas, juntamente com a reavaliação das premissas geocronológicas à luz dos efeitos nucleares de grandes impactos, oferece uma nova e provocadora perspectiva sobre a história da vida na Terra. A hipótese de um catastrofismo radioativo induzido por impactos, capaz de gerar fissão piezonuclear e acelerar o decaimento radioativo, fornece uma explicação coerente para a sincronia de mutações, a preservação anômala de tecidos moles em fósseis e as contradições nas datações radiométricas.
Este modelo integrativo não apenas desafia o uniformitarismo em suas bases, mas também abre novas fronteiras para a pesquisa em paleogenética e medicina de precisão. A compreensão de que a vida na Terra pode ter sido moldada por eventos catastróficos recentes, com consequências genéticas duradouras, nos convida a repensar a nossa própria história evolutiva e a buscar soluções inovadoras para os desafios de saúde e longevidade na era pós-catástrofe genética.
Referências
1.Olivier, M., et al. (2010). TP53 Mutations in Human Cancers. Cold Spring Harbor Perspectives in Biology, 2(1), a001008. PMID: 20182602. PMC: PMC2827900. DOI: 10.1101/cshperspect.a001008. Link
2.Kou, S. H., et al. (2023). TP53 germline pathogenic variants in modern humans were likely originated during recent human history. NAR Cancer, 5(3), zcad025. PMID: 37293531. PMC: PMC10251638. DOI: 10.1093/narcancer/zcad025. Link
3.de Andrade, K. C., et al. (2022). The TP53 Database: transition from the International Agency for Research on Cancer to the National Cancer Institute. Endocrine-Related Cancer, 29(5), R107-R117. PMID: 35254284. PMC: PMC9090805. DOI: 10.1530/ERC-22-0031. Link
4.Joerger, A. C., et al. (2024). TP53: the unluckiest of genes? Nature Reviews Cancer. PMID: 38355745. PMC: PMC11803090. DOI: 10.1038/s41568-024-00662-w. Link
5.Shirole, N. H., et al. (2016). TP53 exon-6 truncating mutations produce separation of function isoforms with tumor-promoting functions. eLife, 5, e19367. PMID: 27760001. PMC: PMC5092050. DOI: 10.7554/eLife.19367. Link
6.Miller, M., et al. (2016). The Evolution of TP53 Mutations: From Loss-of-Function to Gain-of-Function. Cancer Cell, 30(2), 183-185. PMID: 27505677. PMC: PMC5298884. DOI: 10.1016/j.ccell.2016.07.013. Link
7.Belyi, V. A., et al. (2010). The origins and evolution of the p53 family of genes. Cold Spring Harbor Perspectives in Biology, 2(6), a001198. PMID: 20516128. PMC: PMC2874587. DOI: 10.1101/cshperspect.a001198.
8.Fu, W., et al. (2013). Analysis of 6,515 exomes reveals the recent origin of most human protein-coding variants. Nature, 493(7431), 216-220. PMID: 23201682. PMC: PMC3548689. DOI: 10.1038/nature11690.
9.Zhao, B., et al. (2024). Pathogenic variants in human DNA damage repair genes mostly arose in recent human history. BMC Cancer, 24(1), 415. PMID: 38582845. PMC: PMC10998365. DOI: 10.1186/s12885-024-12160-6.
10.Santoni, D., et al. (2021). An entropy-based study on mutational trajectory of SARS-CoV-2 proteins. Scientific Reports, 11, 21644. PMID: 34737341. PMC: PMC8603812. DOI: 10.1038/s41598-021-01124-6. Link
11.Adami, C., et al. (2000). Evolution of biological complexity. PNAS, 97(9), 4463-4468. PMID: 10781047. PMC: PMC18257. DOI: 10.1073/pnas.97.9.4463. Link
12.Zhao, J., et al. (2005). An Entropy-Based Statistic for Genomewide Association Studies. American Journal of Human Genetics, 77(1), 27-40. PMID: 15918152. PMC: PMC1226192. DOI: 10.1086/431160. Link
13.Sherwin, W. B. (2010). Entropy and Information Approaches to Genetic Diversity and its Conservation: Relevance for Management. Entropy, 12(7), 1765-1804. DOI: 10.3390/e12071765. Link
14.Fiscus, C. J., et al. (2025). Mutational load and adaptive variation are shaped by climate and range dynamics in Vitis. PNAS, 122(2), e2411129122. PMID: 39750842. PMC: PMC12177297. DOI: 10.1073/pnas.2411129122. Link
15.Sanford, J. C., et al. (2015). The waiting time problem in a model hominin population. Theoretical Biology and Medical Modelling, 12, 18. PMID: 26376783. PMC: PMC4573302. DOI: 10.1186/s12976-015-0016-z.
16.Eyre-Walker, A., & Keightley, P. D. (1999). High genomic deleterious mutation rates in hominids. Nature, 397(6717), 344-347. PMID: 9950425. DOI: 10.1038/16908.
17.Lynch, M. (2010). Rate, molecular spectrum, and consequences of human mutation. PNAS, 107(3), 961-968. PMID: 20080596. PMC: PMC2824315. DOI: 10.1073/pnas.0912629107.
18.Barboni, M., et al. (2024). High-precision U-Pb zircon dating identifies a major magmatic event on the Moon at 4.338 Ga likely caused by one large impact. Nature Communications, 15, 5945. PMID: 39013921. PMC: PMC11268413. DOI: 10.1038/s41467-024-50232-w. Link
19.Carpinteri, A., & Manuello, A. (2011). Geomechanical and Geochemical Evidence of Piezonuclear Fission Reactions in the Earth’s Crust. Strain, 47(s2), 267-281. DOI: 10.1111/j.1475-1305.2010.00766.x.
20.Carpinteri, A., et al. (2012). Piezonuclear fission reactions in rocks: evidences from microchemical analysis, neutron emission, and geological transformation. Rock Mechanics and Rock Engineering, 45(4), 621-633. DOI: 10.1007/s00603-011-0217-7.
21.Kletetschka, G., et al. (2021). Plasma shielding removes prior magnetization record from impact melt. Scientific Reports, 11, 21544. PMID: 34732761. PMC: PMC8566541. DOI: 10.1038/s41598-021-01451-8.
22.Leckenby, G., et al. (2024). High-temperature 205Tl decay clarifies 205Pb dating in early solar system. Nature Communications, 15, 9412. PMID: 39485721. PMC: PMC11560843. DOI: 10.1038/s41467-024-54179-w.
23.Taleyarkhan, R. P., et al. (2002). Evidence for nuclear emissions during acoustic cavitation. Science, 295(5561), 1868-1873. PMID: 11884748. DOI: 10.1126/science.1067589.
24.Kring, D. A. (2007). The Chicxulub impact event and its environmental consequences. Chemie der Erde – Geochemistry, 67(1), 1-36. DOI: 10.1016/j.chemer.2007.04.002.
25.Morgan, J. V., et al. (2022). The Chicxulub impact and its environmental consequences. Nature Reviews Earth & Environment, 3(4), 232-246. DOI: 10.1038/s43017-022-00283-y.
26.Hawks, J., et al. (2007). Recent acceleration of human adaptive evolution. PNAS, 104(52), 20753-20758. PMID: 18087044. PMC: PMC2410101. DOI: 10.1073/pnas.0707650104. Link
27.Harris, K. (2015). Evidence for recent, population-specific evolution of the human mutation rate. PNAS, 112(11), 3439-3444. PMID: 25733855. PMC: PMC4371947. DOI: 10.1073/pnas.1418652112. Link
28.Harris, K., & Pritchard, J. K. (2017). Rapid evolution of the human mutation spectrum. eLife, 6, e24284. PMID: 28440220. PMC: PMC5435464. DOI: 10.7554/eLife.24284. Link
29.Thomas, G. W. C., & Hahn, M. W. (2014). The human mutation rate is increasing, even as it slows. Molecular Biology and Evolution, 31(2), 253-257. PMID: 24194331. DOI: 10.1093/molbev/mst229. Link
30.Keightley, P. D. (2012). Rates and Fitness Consequences of New Mutations in Humans. Genetics, 190(2), 295-304. PMID: 22345605. PMC: PMC3276617. DOI: 10.1534/genetics.111.134651. Link
31.Henn, B. M., et al. (2015). Estimating the mutation load in human genomes. Nature Reviews Genetics, 16(6), 333-343. PMID: 25963371. PMC: PMC4959039. DOI: 10.1038/nrg3931. Link
32.Simons, Y. B., et al. (2016). The impact of recent population history on the deleterious mutation load in humans. Nature Genetics, 48(3), 284-290. PMID: 26808111. PMC: PMC5161708. DOI: 10.1038/ng.3484. Link
33.McCoy, R. C., et al. (2016). Patterns of deleterious variation between human populations are largely explained by recent history and selection. Genome Biology, 17, 139. PMID: 27357675. PMC: PMC4743776. DOI: 10.1186/s13059-016-1002-8. Link
34.Saclier, N., et al. (2020). Bedrock radioactivity influences the rate and spectrum of spontaneous mutations in Daphnia pulex. Scientific Reports, 10, 21256. PMID: 33277536. PMC: PMC7723406. DOI: 10.1038/s41598-020-78214-w. Link
35.Milián-Sánchez, V., et al. (2020). Fluctuations in measured radioactive decay rates inside a modified Faraday cage: Correlations with space weather. Scientific Reports, 10, 8664. PMID: 32451426. PMC: PMC7244597. DOI: 10.1038/s41598-020-65565-z. Link
36.Medawar, P. B. (1952). An Unsolved Problem of Biology. H. K. Lewis, London.
37.Williams, G. C. (1957). Pleiotropy, Natural Selection, and the Evolution of Senescence. Evolution, 11(4), 398-411. DOI: 10.1111/j.1558-5646.1957.tb02911.x.
38.Kirkwood, T. B. L. (1977). Evolution of ageing. Nature, 270(5635), 301-304. PMID: 593350. DOI: 10.1038/270301a0.
39.Sanford, J. C. (2008). Genetic Entropy & the Mystery of the Genome. FMS Publications.
40.Kondrashov, A. S. (1995). Contamination of the genome by very slightly deleterious mutations: why have we not died 100 times over? Journal of Theoretical Biology, 175(4), 583-594. PMID: 7475094. DOI: 10.1006/jtbi.1995.0167.
41.Kimura, M. (1979). Model of effectively neutral mutations in which selective constraint is incorporated. PNAS, 76(7), 3440-3444. PMID: 291044. PMC: PMC383840. DOI: 10.1073/pnas.76.7.3440.
42.Partridge, L., & Barton, N. H. (1993). Optimality, mutation and the evolution of ageing. Nature, 362(6418), 305-311. PMID: 8455716. DOI: 10.1038/362305a0.
43.Rose, M. R. (1991). Evolutionary Biology of Aging. Oxford University Press.
44.Tyner, S. D., et al. (2002). p53 mutant mice that display early ageing-associated phenotypes. Nature, 415(6867), 45-53. PMID: 11780111. DOI: 10.1038/415045a.
45.Flatt, T., & Promislow, D. E. L. (2007). Still searching for the fountain of youth. Nature, 448(7155), 761-762. PMID: 17700688. DOI: 10.1038/448761a.
46.Schmieder, M., & Kring, D. A. (2020). Earth’s Impact Events Through Geologic Time: A List of Recommended Ages for Terrestrial Impact Structures and Deposits. Astrobiology, 20(1), 91-141. PMID: 31805761. PMC: PMC6987741. DOI: 10.1089/ast.2019.2085. Link
47.Kenny, G. G., et al. (2019). A new U-Pb age for shock-recrystallised zircon from the Lappajärvi impact crater, Finland, and implications for the accurate dating of impact events. Geochimica et Cosmochimica Acta, 245, 479-494. DOI: 10.1016/j.gca.2018.11.013.
48.Moser, D. E., et al. (2011). Zircon U-Pb geochronology of the Maniitsoq structure, Greenland: Evidence for a 3.0 Ga impact event. Earth and Planetary Science Letters, 307(3-4), 305-316. DOI: 10.1016/j.epsl.2011.05.007.
49.Renne, P. R., et al. (2013). Time scales of critical events around the Cretaceous-Paleogene boundary. Science, 339(6120), 684-687. PMID: 23393261. DOI: 10.1126/science.1230492.
50.Schoene, B., et al. (2015). U-Pb geochronology of the Deccan Traps and the Cretaceous-Paleogene mass extinction. Science, 347(6218), 182-184. PMID: 25502315. DOI: 10.1126/science.aaa0118.
51.Burgess, S. D., et al. (2014). High-precision timeline for Earth’s most severe mass extinction. PNAS, 111(9), 3316-3321. PMID: 24516163. PMC: PMC3948271. DOI: 10.1073/pnas.1317692111.
52.Condon, D. J., et al. (2005). U-Pb Ages from the Neoproterozoic Doushantuo Formation, China. Science, 308(5718), 95-98. PMID: 15731406. DOI: 10.1126/science.1107765.
53.Bowring, S. A., et al. (1993). Calibrating Rates of Early Cambrian Evolution. Science, 261(5126), 1293-1298. PMID: 17731845. DOI: 10.1126/science.261.5126.1293.
54.Maloof, A. C., et al. (2010). The earliest Cambrian record of animals and ocean geochemical change and its implications for resolving the Precambrian-Cambrian boundary. GSA Bulletin, 122(11-12), 1731-1774. DOI: 10.1130/B30025.1.
55.Young, G. M. (2013). Evolution of Earth’s atmosphere and the Ediacaran-Cambrian radiation of animals. Geoscience Frontiers, 4(4), 395-412. DOI: 10.1016/j.gsf.2013.01.006.
56.Kaiho, K., et al. (2017). Site of asteroid impact changed the history of life on Earth: the low probability of mass extinction. Scientific Reports, 7, 14855. PMID: 29123110. PMC: PMC5676841. DOI: 10.1038/s41598-017-14199-x.
57.Carlisle, E., et al. (2024). Ediacaran origin and Ediacaran-Cambrian diversification of metazoans. Science Advances, 10(31), eado6462. PMID: 39083611. PMC: PMC11290527. DOI: 10.1126/sciadv.ado6462. Link
58.Wiemann, J., et al. (2018). Fossilization transforms vertebrate hard tissue proteins into insoluble melanin-like polymers. Nature Communications, 9, 4741. PMID: 30413705. PMC: PMC6224595. DOI: 10.1038/s41467-018-07049-x.
59.Schweitzer, M. H., et al. (2005). Soft-tissue vessels and cellular preservation in Tyrannosaurus rex. Science, 307(5717), 1952-1955. PMID: 15790853. DOI: 10.1126/science.1108397.
60.McNamara, M. E., et al. (2010). Organic preservation of fossil musculature with ultracellular detail. Proceedings of the Royal Society B, 277(1680), 423-427. PMID: 19828543. PMC: PMC2842654. DOI: 10.1098/rspb.2009.1378.
61.Surmik, D., et al. (2016). Spectroscopic studies on organic matter from Triassic reptile bones, Upper Silesia, Poland. PLOS ONE, 11(3), e0151143. PMID: 26963215. PMC: PMC4786176. DOI: 10.1371/journal.pone.0151143.
62.Kaye, T. G., et al. (2008). Dinosaurian soft tissues preserved in an extant manner: presence of genomic DNA, proteins and osteocytes. PLOS ONE, 3(7), e2808. PMID: 18665216. PMC: PMC2483347. DOI: 10.1371/journal.pone.0002808.
63.Zou, Y., et al. (2025). Mechanisms of Uranium and Thorium Accumulation in the Lower Ediacaran Marine Sediments from the Doushantuo Formation, South China. Journal of Marine Science and Engineering, 13(3), 413. DOI: 10.3390/jmse13030413. Link
64.Benetti, P., et al. (2019). Neutron emission from fracturing of granite blocks. Physics Letters A, 383(19), 2261-2266. DOI: 10.1016/j.physleta.2019.04.041.
65.Sulak, M., et al. (2016). TP53 copy number expansion is associated with the evolution of increased body size and an enhanced DNA damage response in elephants. eLife, 5, e11994. PMID: 27642012. PMC: PMC5061548. DOI: 10.7554/eLife.11994. Link
66.Nunney, L. (2022). Cancer suppression and the evolution of multiple retrogene copies of TP53 in elephants: a re-evaluation. Evolutionary Applications, 15(6), 910-922. PMID: 35754710. PMC: PMC9108310. DOI: 10.1111/eva.13383. Link
67.Haupt, S., et al. (2017). P53 at the start of the 21st century: lessons from elephants. F1000Research, 6, 2043. PMID: 29225785. PMC: PMC5701437. DOI: 10.12688/f1000research.12344.1. Link
68.Kou, S. H., et al. (2023). TP53 germline pathogenic variants in modern humans were likely originated during recent human history. NAR Cancer, 5(3), zcad025. PMID: 37293531. PMC: PMC10251638. DOI: 10.1093/narcancer/zcad025. Link
69.Li, J., et al. (2025). Pathogenic variation in human DNA damage repair genes was originated from the evolutionary process of modern humans. Genes & Diseases, 12(6), 101916. DOI: 10.1016/j.gendis.2025.101916. Link
70.Chan, Y. L., et al. (2005). Ancient DNA reveals Holocene loss of genetic diversity in a Mauritius kestrel population. Biology Letters, 1(3), 327-330. PMID: 17148199. PMC: PMC1626362. DOI: 10.1098/rsbl.2005.0331. Link
71.Ruiz-Puerta, E. J., et al. (2023). Holocene deglaciation drove rapid genetic diversification of Atlantic walrus. Proceedings of the Royal Society B, 290(2007), 20231349. PMID: 37725831. PMC: PMC10523089. DOI: 10.1098/rspb.2023.1349. Link
72.Hofreiter, M., & Stewart, J. (2009). Ecological Change, Range Fluctuations and Population Dynamics during the Pleistocene. Current Biology, 19(14), R584-R594. PMID: 19640495. DOI: 10.1016/j.cub.2009.06.030.
73.Tan, H. Z., et al. (2023). Megafaunal extinctions, not climate change, may explain Holocene loss of genetic diversity in large mammals. Nature Communications, 14, 4808. PMID: 37558684. PMC: PMC10406428. DOI: 10.1038/s41467-023-40545-w. Link
74.Schreiber, L., et al. (2025). Holocene shifts in marine mammal distributions around the Arctic. Global Change Biology, 31(1), e17651. DOI: 10.1111/gcb.17651. Link
75.Green, R. E., et al. (2010). A Draft Sequence of the Neandertal Genome. Science, 328(5979), 710-722. PMID: 20448196. PMC: PMC5100745. DOI: 10.1126/science.1188021.
76.Prüfer, K., et al. (2014). The complete genome sequence of a Neanderthal from the Altai Mountains. Nature, 505(7481), 43-49. PMID: 24352235. PMC: PMC4031459. DOI: 10.1038/nature12886.
77.Meyer, M., et al. (2012). A High-Coverage Genome Sequence from an Archaic Denisovan Individual. Science, 338(6104), 222-226. PMID: 22936568. PMC: PMC3617501. DOI: 10.1126/science.1224344.
78.Sankararaman, S., et al. (2014). The genomic landscape of Neanderthal ancestry in present-day humans. Nature, 507(7492), 354-357. PMID: 24476815. PMC: PMC4072735. DOI: 10.1038/nature12961.
79.Vernot, B., & Akey, J. M. (2014). Resurrecting Neanderthal Ancestry from the Genomes of Modern Humans. Science, 343(6174), 1017-1021. PMID: 24476670. DOI: 10.1126/science.1245938.
80.Carpinteri, A., et al. (2013). Piezonuclear fission reactions from earthquakes and brittle rocks failure: evidence of neutron emission and non-radioactive product elements. Experimental Mechanics, 53(3), 345-365. DOI: 10.1007/s11340-012-9629-x. Link
81.Carpinteri, A., et al. (2012). Piezonuclear fission reactions in rocks: evidences from microchemical analysis, neutron emission, and geological transformation. Rock Mechanics and Rock Engineering, 45(4), 621-633. DOI: 10.1007/s00603-011-0217-7. Link
82.Carpinteri, A., et al. (2011). Compositional and microchemical evidence of piezonuclear fission reactions in rock specimens subjected to compression tests. Strain, 47(s2), 267-281. DOI: 10.1111/j.1475-1305.2010.00767.x. Link
83.Taleyarkhan, R. P., et al. (2002). Evidence for nuclear emissions during acoustic cavitation. Science, 295(5561), 1868-1873. PMID: 11884748. DOI: 10.1126/science.1067589. Link
84.Taleyarkhan, R. P., et al. (2006). Nuclear emissions during self-nucleated acoustic cavitation. Physical Review Letters, 96(3), 034301. PMID: 16486709. DOI: 10.1103/PhysRevLett.96.034301. Link
85.Ray, A., et al. (2021). Electron capture nuclear decay rate under compression in a confined environment. The European Physical Journal D, 75, 145. DOI: 10.1140/epjd/s10053-021-00145-0. Link
86.Fomitchev-Zamilov, M., et al. (2024). Observation of neutron emission coincident with acoustic cavitation of deuterated titanium powder suspended in mineral oil. Scientific Reports, 14, 11106. PMID: 38745821. PMC: PMC11106313. DOI: 10.1038/s41598-024-61565-x. Link
87.Pommé, S., et al. (2022). Air humidity and annual oscillations in 90Sr decay rate measurements. Scientific Reports, 12, 9184. PMID: 35654821. PMC: PMC9184471. DOI: 10.1038/s41598-022-13244-w. Link
88.Amato, G., et al. (2012). Comment on “Compositional and Microchemical Evidence of Piezonuclear Fission Reactions in Rock Specimens Subjected to Compression Tests”. Strain, 48(4), 357-359. DOI: 10.1111/j.1475-1305.2012.00918.x.
89.Cardone, F., et al. (2009). Piezonuclear neutrons from brittle fracture of iron-rich rocks. Physics Letters A, 373(45), 4158-4163. DOI: 10.1016/j.physleta.2009.09.014.
90.Carpinteri, A., et al. (2014). Piezonuclear fission reactions simulated by the lattice model. Journal of Condensed Matter Nuclear Science, 15, 162-172.
91.Ohtsuki, T., et al. (2004). Enhanced Electron-Capture Decay Rate of 7Be Encapsulated in C60 Cages. Physical Review Letters, 93(11), 112501. PMID: 15447331. DOI: 10.1103/PhysRevLett.93.112501.
92.Jenkins, J. H., et al. (2009). Evidence for Correlations Between Nuclear Decay Rates and Earth-Sun Distance. Astroparticle Physics, 32(1), 42-46. DOI: 10.1016/j.astropartphys.2009.05.004.
93.Fischbach, E., et al. (2009). Time-dependent nuclear decay parameters: new evidence for new forces? Space Science Reviews, 145(3-4), 285-305. DOI: 10.1007/s11214-009-9518-5.
94.Pálffy, A., et al. (2020). Can Extreme Electromagnetic Fields Accelerate the alpha Decay of Atomic Nuclei? Physical Review Letters, 124(21), 212505. PMID: 32530685. DOI: 10.1103/PhysRevLett.124.212505.
95.Mishra, B., et al. (2023). Plasma beta-Decay Rates in the Framework of PANDORA Project. EPJ Web of Conferences, 288, 02001. DOI: 10.1051/epjconf/202328802001.
96.Emery, G. T. (1972). Perturbation of nuclear decay rates. Annual Review of Nuclear Science, 22(1), 165-202. DOI: 10.1146/annurev.ns.22.120172.001121.
97.Timashev, S. F. (2015). Radioactive decay as a forced nuclear chemical process: Phenomenology. Russian Journal of Physical Chemistry A, 89(11), 1903-1910. DOI: 10.1134/S003602441511028X.
98.Kletetschka, G., et al. (2021). Plasma shielding removes prior magnetization record from impact melt. Scientific Reports, 11, 21544. PMID: 34732761. PMC: PMC8566541. DOI: 10.1038/s41598-021-01451-8.
99.Allen, N. H., et al. (2022). A Revision of the Formation Conditions of the Vredefort Crater. Journal of Geophysical Research: Planets, 127(5), e2022JE007186. DOI: 10.1029/2022JE007186.
100.Sodré, G. B. N. (2025). O Evento Catastrófico Holocênico: Piezoeletricidade Nuclear e a Invalidação da Geocronologia Uniformista no Pico Mutacional Humano e em Mamíferos. ResearchGate. DOI: 10.13140/RG.2.2.15799.38563.
101.Sodré, G. B. N., & Siman, H. L. H. B. (2025). As Contradições Datacionais e Geocronológicas Uniformistas (Baseadas em Constância Quase Eterna de Decaimento) Podem Ser Resolvidas pelos Efeitos Nucleares dos Grandes Impactos. ResearchGate. DOI: 10.13140/RG.2.2.35732.21120.
102.Sanford, J. C., et al. (2015). The waiting time problem in a model hominin population. Theoretical Biology and Medical Modelling, 12, 18. PMID: 26376783. PMC: PMC4573302. DOI: 10.1186/s12976-015-0016-z.
103.Behe, M. J. (1996). Darwin’s Black Box: The Biochemical Challenge to Evolution. Free Press.
104.Meyer, S. C. (2013). Darwin’s Doubt: The Explosive Origin of Animal Life and the Case for Intelligent Design. HarperOne.

Deixe um comentário